EU MDR下的UDI实施操作指南
目的: 本指南旨在为医疗器械制造商(特别是对欧盟法规尚不熟悉的制造商)提供一个清晰、分步的操作流程,以正确实施唯一器械标识(UDI)系统,确保符合EU MDR及GS1标准。 第一部分:UDI核心概念解析 在开始操作前,必须清晰地区分UDI系统的三个核心组成部分。混淆这三者是制造商最常犯的错误。 概念 Basic UDI-DI (基础UDI-DI) UDI-DI (器械识别码) UDI-PI (生产
目的:
本指南旨在为医疗器械制造商(特别是对欧盟法规尚不熟悉的制造商)提供一个清晰、分步的操作流程,以正确实施唯一器械标识(UDI)系统,确保符合EU MDR及GS1标准。
第一部分:UDI核心概念解析
在开始操作前,必须清晰地区分UDI系统的三个核心组成部分。混淆这三者是制造商最常犯的错误。
| 概念 | Basic UDI-DI (基础UDI-DI) | UDI-DI (器械识别码) | UDI-PI (生产识别码) |
|---|---|---|---|
| 是什么? | 用于对具有相同预期用途、风险等级、基本设计和制造特性的一组产品进行分组 的主密钥 。 | 用于识别特定制造商的特定型号/版本 医疗器械的唯一编码 。 | 包含器械生产控制信息的动态编码 。 |
| 目的 | 监管目的。 是在EUDAMED数据库中注册器械、关联证书和文档的主标识符。不出现在产品标签上。 | 识别与追溯。 是产品目录、订单、发货和召回中的主要识别码。是UDI标签上的静态部分。 | 生产过程控制。 提供批次、序列号、有效期等信息,实现精准追溯。是UDI标签上的动态部分。 |
| GS1实施 | GMN (全球型号) | GTIN (全球贸易项目代码) ,如GTIN-13, GTIN-14。 | 应用标识符 (AI) + 数据 ,如批号(10)、序列号(21)、有效期(17)等。 |
| 示例 | 制造商的 “A” 系列所有产品 (A1, A2) 共享一个 Basic UDI-DI。 | A1 有一个GTIN,A2有另一个不同的GTIN。 | A1或A2的某个生产批次会有一个特定的批号和有效期。 |
| 完整UDI | 不属于完整UDI的一部分 | 完整UDI = UDI-DI + UDI-PI | 完整UDI = UDI-DI + UDI-PI |
第二部分:UDI合规实施分步操作流程
假设某公司的GS1公司前缀为 69512345 ,它是所有GTIN共有的最长数字串。(注意:695通常代表GS1中国)
步骤 1:产品分组与模型定义 (战略规划)
这是实施UDI的第一步,也是最重要的一步。
- 审查产品线: 梳理所有的医疗器械产品。
- 依据MDR进行分组: 根据MDR附录VI C部分的定义,将具有相同预期用途、风险等级、基本设计和制造特性的产品划分为一个“模型/家族”,即国内所说的注册单元。
- 示例: 型号A1、A2 因核心设计与用途相同,归为 “A模型” 。B1 是一个独立模型。
- 结论: 您需要创建2个 不同的Basic UDI-DI。
步骤 2:创建并分配 Basic UDI-DI (GMN)
为上一步定义的每个“模型”创建一个Basic UDI-DI。以 “A模型” 为例。
定义“模型参考号 (Model Reference)”:
- 基于GS1公司前缀 69512345,为 “A模型” 定义一个有意义且唯一的模型参考号。
- 最佳实践: 建议使用 ModelA。它简洁、易于理解且符合GS1规范[可以使用字母(A-Z,区分大小写)和数字(0-9)]。
- 此时,得到一个待计算的字符串:69512345ModelA
计算“校验码 (Check Characters)”:
- 访问 GS1官方校验码计算器 :https://www.gs1.org/services/check-character-calculator
- 在页面中,选择标识符类型为 GMN (Global Model Number) 。
- 在输入框中,输入刚才组合的字符串:69512345ModelA
- 点击计算。工具会自动生成两位 校验码。请准确记录下来(例如,本示例中工具生成了 EJ)。

形成并记录完整的Basic UDI-DI:
- 将三部分组合:[GS1公司前缀] + [模型参考号] + [计算出的校验码]
- 最终结果: “A模型”的Basic UDI-DI为 69512345ModelAEJ。
- 重要: 将此结果记录在技术文档和质量管理体系(QMS)中,并用于后续的EUDAMED数据库注册。
- 重复此过程 为“B模型”或其他模型创建它们各自的Basic UDI-DI。
步骤 3:创建并分配 UDI-DI (GTIN)
为每个可单独销售或使用的具体产品规格 分配一个唯一的UDI-DI。
确定分配对象: 在 “A模型” 内部,A1, A2 是不同的产品规格,因此每一个都需要一个独立的GTIN 。
分配物项号: 在公司前缀 69512345 后面,为每个产品分配一个内部不重复的物项号。
- A1 物项号 0006 -> 组合为 695123450006
- A2 物项号 0007 -> 组合为 695123450007
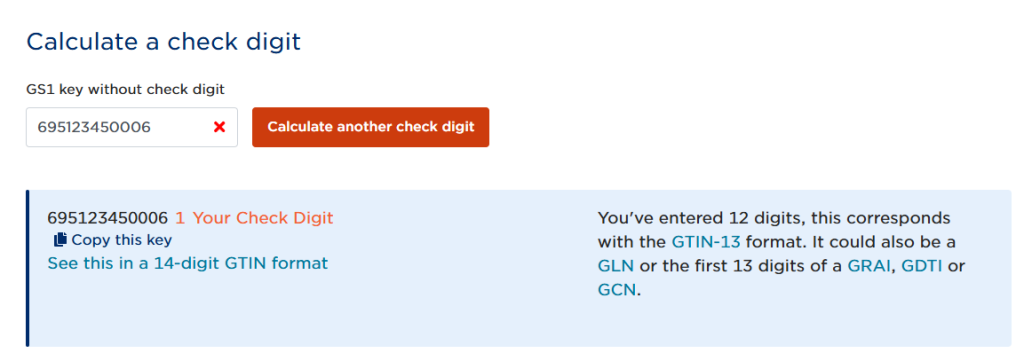
计算GTIN校验位: 使用GS1校验码计算器(选择GTIN类型 https://www.gs1.org/services/check-digit-calculator)为上述每个组合计算一位 的校验位。
例如,695123450006 的校验位是1。
形成完整的UDI-DI (GTIN):
- A1 的UDI-DI是 6951234500061
- A2 的UDI-DI是 6951234500078
注意: 如果使用包装层级指示符(如外箱),会形成GTIN-14,例如 0 6951234500061。
步骤 4:确定并应用 UDI-PI (生产标识)
在生产线上,为每个(或每批)产品附加生产信息。
确定必需的PI: 根据器械风险等级和类型,MDR要求可能包括:
- (10) 批号 (Lot/Batch Number)
- (21) 序列号 (Serial Number)
- (17) 有效期 (Expiration Date)
- (11) 生产日期 (Manufacturing Date)
应用到产品: 在生产过程中,将这些动态数据赋给每个产品或批次。
步骤 5:生成UDI载体并提交数据
生成UDI载体: 将UDI-DI和UDI-PI组合,并以人眼可读(纯文本)和机器可读(如GS1-128条码、DataMatrix码)的形式呈现在产品标签和各级包装上。
GS1-128条码内容示例: (01)06951234500061(17)280515(10)LOT12345
- (01): GTIN的AI(应用标识符,用于标识条形码或标签中编码的数据类型)
- 06951234500061: 完整的GTIN-14
- (17): 有效期的AI
- 280515: 有效期 (YYMMDD格式)
- (10): 批号的AI
- LOT12345: 批号
提交数据至EUDAMED: 将您的Basic UDI-DI和所有相关的UDI-DI数据按要求提交至欧盟医疗器械数据库(EUDAMED)。
第三部分:最佳实践与常见误区
最佳实践
- ✅ 规划先行,策略至上: 在生成任何编码前,先完成第一步的产品分组。这是所有后续工作的基础。
- ✅ 建立中央UDI数据库: 在企业内部建立一个统一的数据库或管理系统,记录所有Basic UDI-DI和UDI-DI的分配情况、关联关系及生命周期状态。
- ✅ 融入质量管理体系(QMS): 将UDI的创建、分配、变更和停用流程正式纳入的QMS文件,确保操作的一致性和合规性。
- ✅ 全员培训: 确保研发、生产、质量、法规、销售等所有相关部门的员工都理解UDI的基本概念和他们在流程中的职责。
- ✅ 版本控制: 对UDI数据记录进行严格的版本控制,尤其是在产品发生变更时。
常见误区
- ❌ 混淆三个“DI”: 不要将Basic UDI-DI打在产品标签上,也不要为一个模型的不同规格使用相同的UDI-DI。
- ❌ 随意编造校验码: 校验码必须通过官方工具计算,随意填写的编码是无效的。
- ❌ 忽视UDI-PI: UDI-DI只是“身份证号”,没有UDI-PI就无法实现精准批次追溯,不符合MDR要求。
- ❌ 编码后即忘: 创建UDI编码只是第一步,后续的数据维护、标签应用、数据库提交以及在供应链中的使用同样重要。
- ❌ 变更管理混乱: 当产品发生需要变更UDI-DI或Basic UDI-DI的重大设计变更时,必须严格按照法规和内部流程执行,分配新的编码,而不是修改旧的。

